 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是()
A.向水中投入一小块金属钠
B.将水加热煮沸
C.向水中通入二氧化碳气体
D.向水中加食盐晶体
 答案
答案
向水中通入二氧化碳气体
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.向水中投入一小块金属钠
B.将水加热煮沸
C.向水中通入二氧化碳气体
D.向水中加食盐晶体
 答案
答案
向水中通入二氧化碳气体
 更多“能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是()”相关的问题
更多“能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是()”相关的问题
第1题
A.中和同体积同浓度的HAc和HCl,所需碱量是相同的
B.由H2CO3的解离平衡,可知溶液中H+]和CO32-]的比值=2∶1
C.血液中HCO3-]和CO32-]的比值达到20/1,但由呼吸作用和肾的生理功能的补充或调节,使HCO3-和CO2溶解的浓度保持相对稳定而使血浆中的碳酸缓冲系具有缓冲能力
D.缓冲容量β越大,溶液的缓冲能力越强
第3题
A.能电离出氢离子和酸根离子的化合物叫做酸
B.盐电离时生成的阳离子只有金属离子
C.碱电离时生成的阴离子只有OH-离子
D.酸、碱在不溶液中电离生成的阴、阳离子数目相等,所以整个溶液不显电性
第4题
A.玻璃电极在强酸溶液中被腐蚀
B.H+与H2O形成H3O+,结果降低,pH增高
C.H+度高,它占据了大量交换点位,pH值偏低
D.在强酸溶液中水分子活度减小,使H+传递困难,pH增高
第5题
A.玻璃膜在强碱性溶液中被腐蚀
B.强碱性溶液中Na+浓度太高
C.强碱性溶液中OH-中和了玻璃膜上的H+
D.大量OH-占据了玻璃膜上的交换占位
第6题
以下试验现象,与新制氯水中的某些成分(括号内物质)没有关系的()。
A.将NaHCO3固体参加新制氯水,有无色气泡(H+)
B.使红色布条褪色(HCl)
C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发觉呈血红色(Cl2)
D.滴加AgNO3溶液生成白色沉淀(Cl-)
第7题
A.①→③→④→②
B.①→③→②→④
C.①→②→③→④
D.①→④→②→③
第8题
第9题
最近科学家提出“绿色自由”设想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。“绿色自由”设想技术流程如下
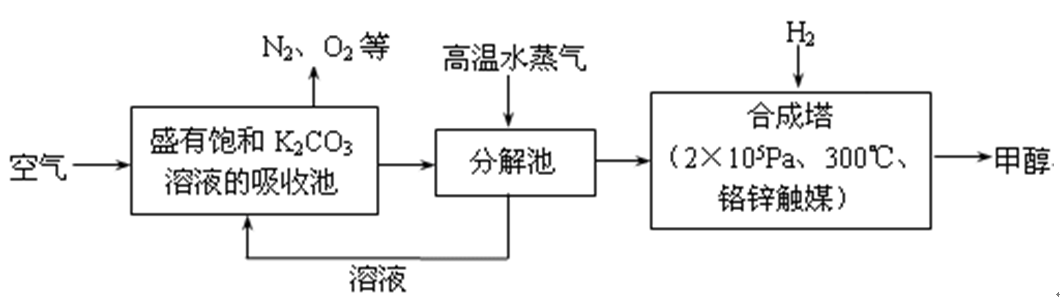
问题一、分解池中发生分解反应的物质是()。
问题二、在合成塔中,假设有CO2与足量H2kJ的热量,试写出合成塔中发生反应的热化学方程式()
问题三、①从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300℃的温度,原因之一是考虑到催化剂的催化活性,原因之二是()。
②“绿色自由”设想技术流程中常包括物质和能量的“循环利用”,上述流程中能表达“循环利用”的除碳酸钾溶液外,还包括()。
问题四、右图是甲醇燃料电池的结构示意图。已知电池总反应为:2CH3OH+3O2=2CO2+4H2O。通入a一端的电极是(填“正极”或“负极”),负极发生的电极反应是()。
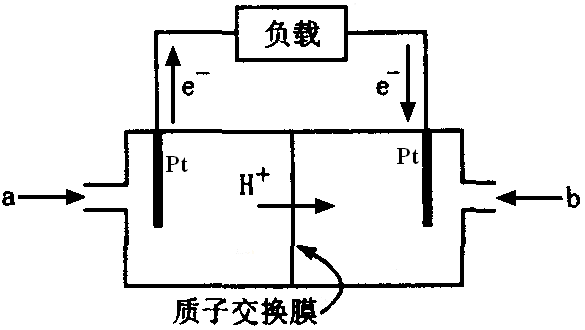 答案:
答案:
第10题
A.某一化合物,在任何情况下,其电离平衡不会移动
B.电离平衡是一种动态平衡
C.在达到电离平衡时,应马上停止
D.任何化合物在水中都存在着电离平衡
第11题
A.在单凝聚法中加入硫酸钠主要是增加溶液的离子强度
B.在沉降囊中调节pH值到8~9,加入37%甲醛溶液于15℃以下使微囊固化
C.影响成囊因素除凝聚系统外还与明胶溶液浓度及温度有关
D.单凝聚法是相分离法常用的一种方法
E.单凝聚法中调节pH至明胶等电点即可成囊